Intervenire sulla rottura operata dal Plasmodium come nuovo trattamento per la malaria
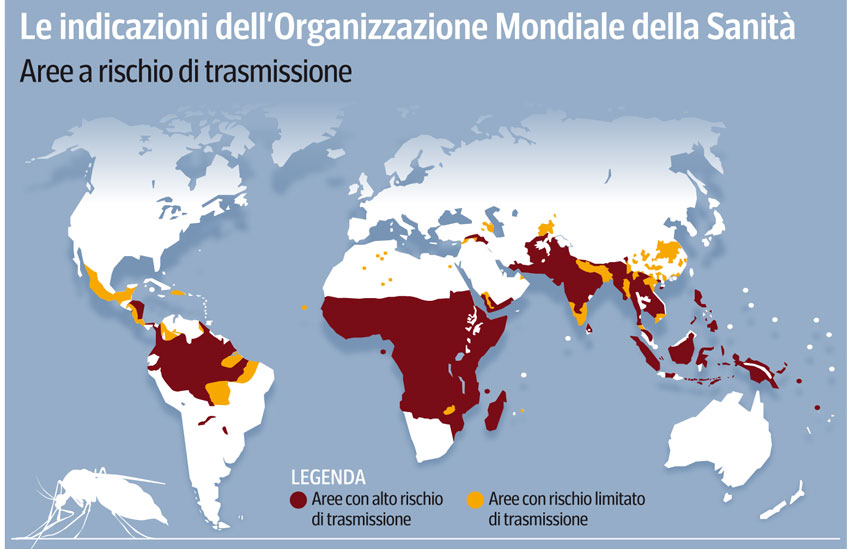
La malaria continua ad essere una principale sfida sanitaria per i paesi in via di sviluppo, causando circa mezzo milione di decessi ogni anno. Per affrontare la mancanza di vaccini e l’affermarsi della resistenza contro i farmaci esistenti, i ricercatori europei hanno esaminato un passaggio chiave nel ciclo di vita del parassita.
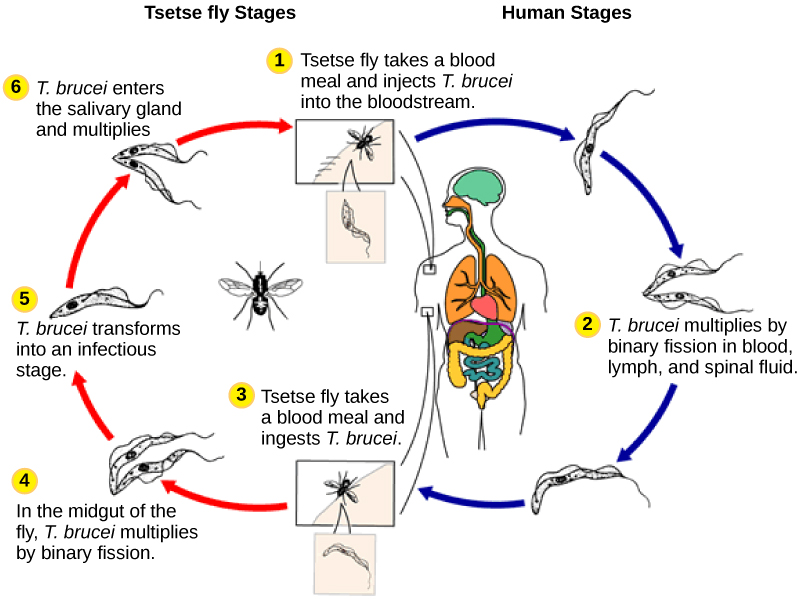
Quando i parassiti della malaria invadono i globuli rossi (RBC, Red Blood Cells) ospiti, si racchiudono all’interno di un compartimento legato alla membrana conosciuto come vacuolo parassitoforo. Circa 48 ore dopo, una volta terminato il proprio ciclo di crescita asessuata nello stadio ematico, il parassita rompe la membrana in modo coordinato prima di uscire dagli RBC, un processo noto come rottura.
Attualmente, il meccanismo attraverso cui i parassiti della malaria rompono questa membrana è completamente sconosciuto, ma è fondamentale per la riproduzione dei parassiti. Al contempo, considerata la nota capacità dei parassiti del Plasmodium di sviluppare rapidamente la resistenza contro i farmaci antimalarici, si avverte il bisogno urgente di identificare nuovi bersagli farmacologici e superare l’efficacia limitata delle soluzioni esistenti.
Il ruolo svolto dagli enzimi che rompono la membrana nell’uscita dei parassiti
Intrapreso con il supporto del programma Marie Skłodowska-Curie, il progetto MalariaEgress, situato nel laboratorio ospitante di Mike Blackman presso l’Istituto Francis Crick nel Regno Unito, ha lavorato all’ipotesi secondo cui il parassita della malaria deve utilizzare un tipo di enzima che rompe la membrana, chiamato fosfolipasi, per uscire dagli RBC. «La malaria è un’epidemia in corso, quindi si avverte una forte esigenza di identificare nuovi bersagli farmaceutici coinvolti in processi cruciali nel ciclo di vita dei parassiti», sottolinea Abhinay Ramaprasad, borsista di ricerca.
Nel parassita della malaria sono presenti 23 diverse fosfolipasi potenzialmente coinvolte nella sintesi e nella rottura dei fosfolipidi del vacuolo parassitoforo. Gli scienziati hanno impiegato il knockout dei geni e le tecnologie di editing genetico, quali CRISPR-Cas9, per rompere tali geni e, in seguito, hanno eseguito un esame estensivo dell’impatto del knockout sulla capacità del parassita di crescere, moltiplicarsi e uscire dagli RBC. L’analisi dei lipidi prodotti dal parassita ha permesso loro di determinare la funzione delle fosfolipasi in fase di studio.
Per la durata del progetto, Ramaprasad ha caratterizzato le funzioni di quattro fosfolipasi e scoperto che svolgono un ruolo in diversi punti del ciclo di vita del parassita nel sangue. Due enzimi sono risultati essenziali per la crescita dei parassiti, mentre un altro si è rivelato necessario per la rottura efficiente, suggerendo una loro possibile funzione come bersagli terapeutici per lo sviluppo di un nuovo farmaco antimalarico. Di particolare interesse è il fatto che la fosfolipasi che aiuta il parassita a uscire in modo efficiente funziona modificando la membrana vescicolare che lo circonda, rendendola più soggetta alla rottura.
Significato e prospettive del progetto
La ricerca verso nuovi trattamenti per la malaria è fondamentale. «Gli enzimi che includono le fosfolipasi costituiscono bersagli eccellenti per i farmaci contro i patogeni causa di importanti malattie infettive», evidenzia Ramaprasad. Alcuni importanti esempi includono la proteasi dell’HIV e il virus dell’influenza neuraminidasi, bersagli di farmaci di successo a livello clinico. Sulla base di ciò, MalariaEgress ha ricercato la biologia fondamentale alla base della proliferazione del parassita e della patogenesi della malaria con l’intenzione di sviluppare nuovi farmaci.
I risultati del progetto sveleranno il ruolo chiave delle fosfolipasi nelle dinamiche di membrana richieste per il ciclo di vita ematico asessuato del parassita, tra cui l’uscita dagli RBC. Con uno sguardo al futuro, Ramaprasad sottolinea che «le attività si concentreranno sull’intervenire su queste fosfolipasi essenziali con piccole molecole simili a farmaci sicure per l’utilizzo umano».